Une syncope est une « perte de connaissance totale, transitoire, secondaire à une hypoperfusion cérébrale, de durée brève, spontanément résolutive avec retour à un état de conscience normal » (ESC 2018 [1]). Ce symptôme est fréquent, sa prévalence est de l’ordre de 30 % dans la population générale [1bis]. Elle représente 1 à 6 % des consultations médicales et plus de 3 % des admissions en service d’urgence. Aux États-Unis, 30 à 40 % des patients se présentant en service d’urgence pour syncope sont admis en hospitalisation [1bis].
Perte de connaissance, malaise, lipothymie, évanouissement, pré-syncope (anglo-saxon) ou coma ne sont pas synonymes de syncope, car ils peuvent être dus à une commotion cérébrale (trauma crânien suivi de PC), une cause médicamenteuse ou toxique, une cause psychogénique ou neurologique comme un AVC, une amnésie (ictus) ou une crise comitiale et autres causes rares (cf. Syncope. étiologies).
Étiologies
On distingue trois groupes étiologiques [1][4]
1 – Les syncopes réflexes (les plus fréquentes)
2 – Les syncopes par hypotension orthostatique
3 – Les syncopes cardiovasculaires
-
- les causes rythmiques (cf. Syncope rythmique)
- les causes mécaniques structurelles (sténose aortique sévère, embolie pulmonaire, CMH, myxome et autres tumeurs de l’oreillette, tamponnade, HTAP, dissection aortique, dysfonction de prothèse valvulaire…).
Le schéma ci-dessous décrit l’ensemble des facteurs déclenchants et favorisants une syncope (ESC 2018)
Une syncope a-t-elle un mauvais pronostic ?

Le pronostic de la syncope est extrêmement variable en fonction de la cause. Dans la cohorte de Framingham (7814 participants, 51 ± 14.4 ans; suivi moy. 17 ans) [22], 21 % ont pour cause un mécanisme vasovagal, 9,5 % une origine cardiaque, 9,4 % une hypotension orthostatique, la syncope restant de cause indéterminée dans 36 % des cas.
Les personnes souffrant de syncope cardiaque courent un risque accru de décès et d’événements cardiovasculaires quelle qu’en soit la cause, et les personnes souffrant d’une syncope de cause inconnue courent un risque accru de décès quelle qu’en soit la cause. La syncope vasovagale et l’hypotension orthostatique semblent avoir un pronostic bénin à long terme. La recherche d’une étiologie cardiovasculaire est donc primordiale (coronaire, obstructive valvulaire, péricardique, musculaire type CMO, aorte ou artère pulmonaire ou bien une arythmie) ! Syncope. Étiologies (ESC 2018).
Les études pronostiques réalisées sur la syncope aux urgences montrent que des événements cliniques graves surviennent souvent très précocement après la première évaluation, souvent dans les 48 premières heures. Les taux d’événements graves survenant dans les 7 à 31 jours suivant l’admission peuvent varier entre 7 et 23 % selon les études [21].
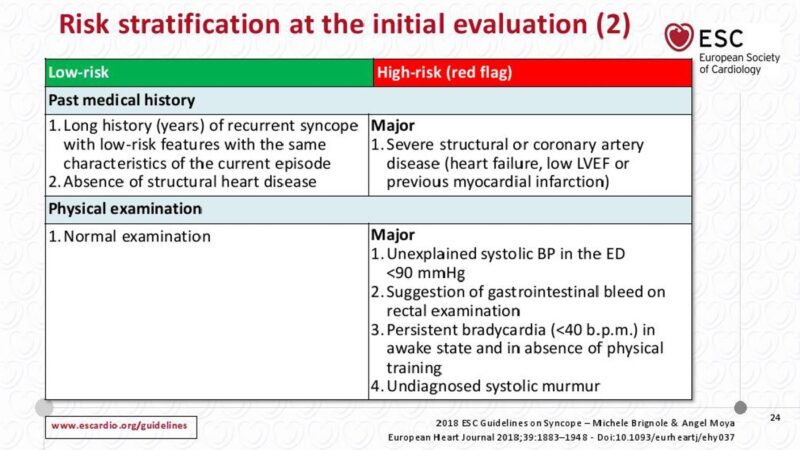
En première approche, il ressort des principaux scores de stratification du risque [21] que :
- les trois principaux critères de gravité immédiats reconnus par la SFMU en 2005 [2bis] sont : l’âge (le sujet âgé ≥ 60 ans), une syncope brutale « à l’emporte-pièce », une étiologie cardiaque connue ou probable. Pour les auteurs de ces recommandations, tout malaise doit être exploré comme une syncope, car en partage le même pronostic [2bis].
- des critères plus précis définis en 2018 par la SFC intègrent des éléments liés à la sémiologie de l’évènement syncopal, les antécédents et l’examen physique [1].
- l’ECG est indispensable pour affiner le niveau de risque [1]. Ces experts ajoutent qu’il faut monitorer (scope/télémétrie) immédiatement les patients à haut risque de syncope rythmique (durant le temps de la prise en charge jusqu’à complète l’évaluation).

NB. D’autres critères sont importants pour décider d’une hospitalisation : un traumatisme secondaire (« injury caused by syncope« ), une pathologie « lourde » associée ou une polypharmacie, un besoin d’évaluation diagnostique rapide ou de traitement spécifique, une répétition rapprochée des syncopes [1]…
Ne sous-estimez pas la gravité d’une syncope parce que le patient a rapidement repris conscience
YouTube (P Taboulet, 22 min)
Prise en charge médicale
Des recommandations formulées en 2018 par la Société européenne de Cardiologie (ESC) sur la prise en charge des syncopes existent et sont régulièrement actualisées (lire diaporama complet de la ESC [1] et autres réf. [2]). Elles sont indispensables à connaître pour comprendre tous les mécanismes qui concourent à leur survenue (cf. Syncope. Étiologies), guider le clinicien dans son diagnostic et la reconnaissance des formes potentiellement les plus à risque d’évènement grave (récidive, mort subite…). Les recommandations de la Société française de médecine d’Urgence sont plus spécifiquement adressées aux urgentistes et l’approche, différente, est, elle aussi, intéressante (SFMU 2005 [2bis] et Taboulet P 2019 [20]).
En pratique, on constate, hélas, que la prise en charge des syncopes est hétérogène, très dépendante de la qualité du premier contact médical. Le triage par téléphone est un exercice périlleux, car une bonne évaluation comprend au minimum un interrogatoire, un examen physique et un ECG (voir tableau ci-dessous [20]). La méticulosité et l’expérience sont indispensables (pour moi la syncope est un des problèmes les plus complexes de la médecine de premier recours).
PT. Il est prudent de considérer qu’une syncope est cardiaque jusqu’à preuve du contraire. De plus, avant évaluation médicale, il me paraît prudent de laisser allongé le patient qui a syncopé tant que les paramètres vitaux n’ont pas été recueillis et qu’une embolie pulmonaire n’a pas été écartée, en particulier chez les sujets âgés (PT vidéo : YouTube) chez qui la prévalence de l’EP est élevée autour de 80 ans [25] et le risque d’hypotension orthostatique ou de blessure en cas de chute est plus élevé.
La première étape clinique est un interrogatoire « policier »
L’interrogatoire du patient et d’éventuels témoins doit permettre de reconstituer méticuleusement le déroulement de la syncope : circonstances de survenue, recherche de prodromes, signes accompagnant le malaise/syncope et mode de terminaison/évolution sont essentiels (le QUOI, le QUAND, le COMMENT). Il doit aussi permettre de préciser le QUI : âge, antécédents, épisodes similaires, comorbidités et médicaments. La notion de comorbidité sévère (cœur, poumon, neuro, anémie, dysautonomie…) ou de polypharmacie (cardio, neuro ou L-dopa) ne doit focaliser uniquement l’attention sur ces pistes [1]. Les données à rechercher sont particulièrement bien développées dans ce document (SFMU 2005) [2bis] et Taboulet 2019 [20].
Au terme de l’interrogatoire, il est généralement possible de s’orienter vers un mécanisme étiologique si certaines particularités sont présentes dans l’anamnèse [20].

a. Syncopes réflexes de type malaise vasovagal.
b. Syncopes situationnelles.
c. Syncope par hypersensibilité du sinus carotidien (voir « Massage du sinus carotidien »)
d. Principalement des antihypertenseurs, mais aussi des dérivés nitrés, des alpha‐1 bloquants pour le traitement de l’hypertrophie bénigne de prostate, du sildénafil, de collyre antiglaucomateux, antiparkinsoniens, anticholinergiques, opiacés…
e. L’hypotension orthostatique neurogène est habituellement associée à une absence d’augmentation de la fréquence cardiaque en orthostatisme.
L’interrogatoire ne permet pas toujours de classer dans une de ces trois catégories le symptôme initial. Ainsi, certaines syncopes prolongées se terminent par des mouvements tonico-cloniques [27], ce qui peut égarer vers le diagnostic d’épilepsie si la chronologie « perte de connaissance durable, puis mouvements anormaux, puis récupération complète et rapide » n’est pas établie. D’autres syncopes se compliquent de traumatismes crâniens avec amnésie antérograde, ce qui rend le diagnostic causal incertain. Enfin, l’interrogatoire du sujet âgé ou des sujets aux fonctions cognitives déficitaires est parfois sujet à caution. Toute chute chez une personne âgée doit faire rechercher activement un malaise cardiaque avant la chute et toutes les causes de malaise doivent être explorées [2].
La seconde étape est un examen physique complet
La recherche d’une maladie cardiaque est particulièrement cruciale, car les patients « cardiaques » sont les plus à risque de décès.
- L’attention doit être dirigée initialement vers les signes vitaux, l’examen cardiovasculaire, respiratoire et neurologique. Il faut rechercher ensuite des signes en faveur d’une étiologie pulmonaire (ex. embolie), une anémie profonde, une hémorragie interne (digestive), un toxidrome (drogues, monoxyde de carbone…). L’examen doit rechercher aussi des signes de traumatisme lié à la chute, ce qui constitue un critère de gravité .
- L’échographie clinique (≠ échocardiographie) est un outil diagnostique incontournable si l’évaluation initiale de la volémie, des cavités cardiaques et du péricarde s’avère nécessaire [6][7]. Elle n’est pas recommandée de façon systématique pour toute syncope, mais à la moindre suspicion de syncope cardiaque. Elle peut permettre rapidement d’établir des diagnostics rares (sténose aortique sévère, ischémie coronaire aiguë, cardiomyopathie hypertrophique ou obstructive, tamponnade, myxome ou thrombus de l’oreillette, dysfonction de prothèse valvulaire, embolie pulmonaire, hypertension artérielle pulmonaire, dissection aortique).
La troisième étape est la réalisation d’un électrocardiogramme (ECG)
L’ECG a une rentabilité faible (3-5%), mais la gravité et la surmortalité des causes cardiaques justifient sa réalisation systématique. Un avis cardiologique en urgence peut être justifié pour préciser l’existence et la sévérité potentielle d’une anomalie constatée.
- Avant l’ECG, on peut utiliser temporairement les valeurs de fréquence cardiaque affichées sur un tensiomètre ou un saturomètre en oxygène ; néanmoins ces appareils ne détectent que l’onde de pouls et peuvent sous-estimer les fréquences cardiaques rapides ou irrégulières, comme celles d’une fibrillation atriale ou d’un bigéminisme atrial ou ventriculaire.
- L’ECG doit être réalisé précocement après le début des symptômes. Il doit être lu attentivement et décrit parfaitement dans le dossier du patient (Rythme et FC, conduction AV, complexes QRS, repolarisation et QT). Plusieurs ECG consécutifs sont parfois nécessaires pour enregistrer la cause éventuelle de la syncope, voire un monitorage chez les patients à haut risque.
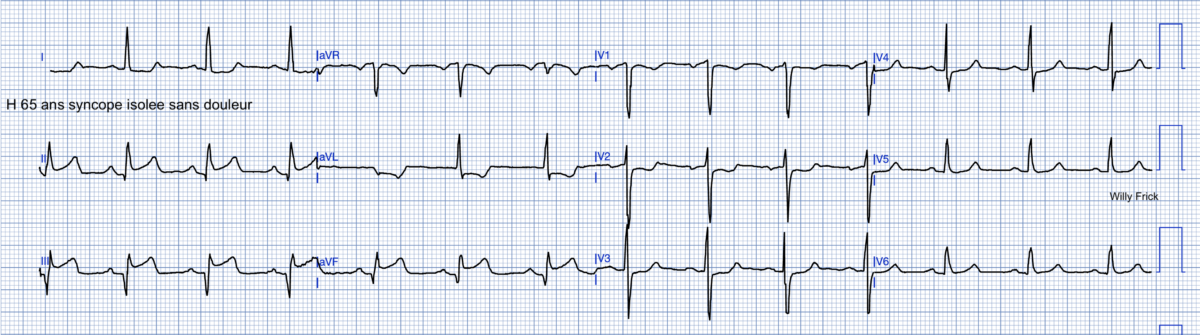
H 65 ans, ECG juste après syncope, sans prodrome ni symptôme ultérieur : infarctus par occlusion CD
- Certaines anomalies sont associées à un haut risque de récidive(s) ou de complication(s) ; d’autres anomalies sont associées à un risque mineur, sauf si la clinique évoque une syncope arythmique (palpitations préalables, douleur thoracique, syncope « à l’emporte-pièce ») (cf. ci-dessous) [1]. –> Lire syncope rythmique.
* risque mineur (haut risque si anamnèse en faveur d’une syncope rythmique).
BAV = bloc atrioventriculaire ; bpm = battements par minute ; CAVD = cardiomyopathie arythmogène du ventricule droit ; ECG = électrocardiogramme.
- La mesure de l‘intervalle QT puis le calcul de l’intervalle QTc sont indispensables. Toute syncope (ou épisode atypique de convulsions) en présence d’un intervalle QT long doit faire suspecter des torsades de pointes. Un QTc > 460 ms est à risque et > 500 ms à haut risque, car il indique un syndrome du QT long (en cas de QRS ≤ 120 ms) [1]. Les valeurs de QTc calculées par les ordinateurs sont généralement fiables quand le rythme est stable et la fréquence cardiaque proche de 60/min. Néanmoins, quand le rythme est variable, les QRS larges ou l’onde T mal discernable, les valeurs proposées peuvent être fausses, c’est pourquoi il est recommandé de les valider par une mesure manuelle du QT. De plus, la valeur du QTc peut varier significativement quand la fréquence cardiaque s’écarte trop de 60/min (ex ≤ 50/min ou ≥ 90/min) selon la formule utilisée. Ainsi, la formule de Bazett sous-estime significativement les valeurs de QTc dans les fréquences basses (ex. < 50/min) et les surestime dans les fréquences hautes (ex. > 90/min) par rapport aux autres formules (Fridericia, Hodges…). La fréquence cardiaque et la formule de calcul du QTc affichée par l’ordinateur doivent donc être précisées dans le compte rendu de lecture.
- Il est rare de pouvoir enregistrer sur l’ECG l’anomalie rythmique précise qui explique la syncope. C’est pourquoi un monitorage ECG (scope ou télémétrie, dès que possible) est recommandé quand il y a un « haut risque » de syncope rythmique (ESC 2018, Classe I, C [1]). Ce monitorage peut augmenter les chances de détection d’une anomalie rythmique en particulier si le patient a présenté des palpitations, une gêne thoracique, une dyspnée, une syncope à l’emporte-pièce (cf.), qu’il a un terrain cardiovasculaire (en particulier ischémique), qu’il a des anomalies ECG à haut risque ou un pacemaker/défibrillateur.
- Aux porteurs de pacemaker, on peut proposer un « test à l’aimant » quand l’électrostimulation est invisible, intermittente ou anormale sur l’ECG initial ou au cours du monitorage. Certains dysfonctionnements de pacemaker peuvent entrainer des malaises/syncopes comme un défaut de stimulation, une tachycardie par réentrée électronique, ou d’autres arythmies [11]. Leurs diagnostics nécessitent généralement l’avis du cardiologue rythmologue référent (qui pourra, de plus, interroger le PM pour analyser rétrospectivement le rythme au cours de la syncope).
La quatrième étape comprend des examens complémentaires
Leur séquence est guidée par les hypothèses formulées au terme des premières étapes. Aucune série de test n’est universellement applicable.
Les tests sanguins sont réalisés quand indiqués cliniquement [1] : glycémie capillaire chez le diabétique, hémoglobine et hématocrite quand une anémie ou une hémorragie est suspectée, saturation cutanée en oxygène ou analyse des gaz du sang quand une hypoxie est suspectée, D-dimères quand une embolie pulmonaire est suspectée, NT-probnp quand une insuffisance cardiaque est suspectée et troponine quand des symptômes douloureux cardiaques précèdent le syncope [24], un dosage de l’HbCO etc.
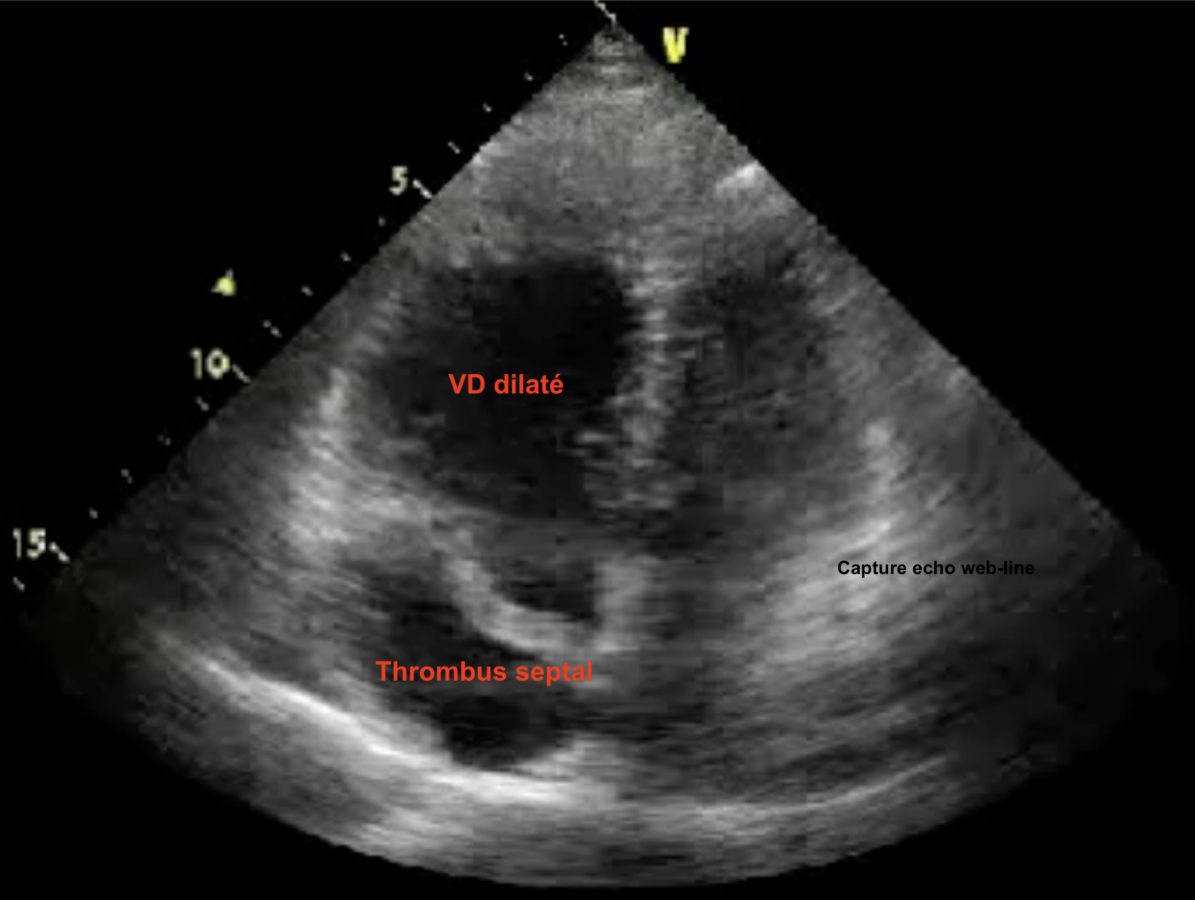
L’échocardiographie transthoracique – en l’absence d’élément d’orientation clinique ou électrocardiographique en faveur – ne révèle généralement pas d’arguments pour une syncope cardiaque structurelle ou cardio-pulmonaire. Ce n’est pas un test systématique en cas de syncope [1][3]. En présence d’éléments d’orientations (dyspnée, souffle systolique, signes congestifs…) il est important qu’une échocardiographie au lit du malade soit réalisée au lit du malade dès la fin de l’étape 3. Elle peut révéler la cause structurelle cardiaque ou pulmonaire de la syncope (cf photo d’une dilatation du VD au cours d’une EP massive avec thrombus septal, image echo web-line).
La cinquième étape comprend deux autres tests diagnostiques cliniques
En l’absence de diagnostic établi lors des précédentes étapes, ces tests sont indispensables selon les hypothèses physiopathologiques. Ils doivent être réalisés et interprétés « proprement » pour :
A – La recherche d’une hypotension orthostatique (HO). Cette recherche est recommandée dans l’évaluation initiale d’une syncope (classe IC) (1), en particulier après 65 ans ou état morbide favorisant (cf. supra). Elle repose sur une technique rigoureuse et ne doit pas être déléguée à un tiers qui n’est pas parfaitement formé à la recherche d’une HO.
- Le patient est allongé à plat pendant une période suffisamment longue avant le test (ex. > 5-10 min), de préférence au calme et sans parler. Les mesures de tension artérielle et de fréquence cardiaque sont débutées au terme de cette période en position couchée, puis renouvelées immédiatement après obtention de la position debout (ou à défaut la position assise) de façon active (le patient doit se lever lui-même) [4]. Si une hypotension n’est pas détectée précocement, les mesures doivent être répétées plusieurs fois jusqu’à la fin de la 3e minute. Les tensions systolique/diastolique et la fréquence cardiaque doivent être notées à chaque fois. La chute de la tension artérielle est parfois maximum (≥ 50 mmHg) dans les 15 premières secondes [12]. Il est nécessaire de rester près du patient en raison du risque de chute et de l’interroger sur les symptômes qu’il ressent pendant le test.
- La méthode diagnostique recommandée par l’ESC repose sur la pose d’un brassard à tension adapté à la circonférence du bras du patient et muni d’un sphygmomanomètre (tensiomètre manuel). Cette méthode permet d’analyser à l’aide d’un stéthoscope posé sur la zone humérale, au-dessous du brassard, les bruits de Korotkoff. Lors du dégonflage progressif du brassard, l’apparition des bruits correspond à la valeur de tension artérielle systolique (la plus discriminante). Les mesures obtenues par un brassard automatique à tension ne permettent pas l’obtention de valeurs dès le début de l’orthostatisme (1,12), mais sont acceptables [4].
- La valeur de tension artérielle systolique la plus basse est retenue. Une chute anormale de TA est définie comme une baisse importante de la TA systolique par rapport à la valeur initiale > 20 mmHg ou de la TA diastolique > 10 mmHg, ou une diminution de la TA systolique < 90 mmHg chez les patients avec une TA en décubitus < 110 mmHg [1]. Une baisse isolée de la TA diastolique est très rare et sa pertinence clinique pour le diagnostic d’une HO est limitée. L’augmentation de la fréquence cardiaque orthostatique est habituelle. Elle peut être faible ou absente [habituellement pas > 10 battements par minute (bpm)] chez les patients avec HO neurogène, ou exagérée en cas d’anémie ou hypovolémie.
- Le diagnostic d’HO est posé si les symptômes coïncident avec la constatation d’une HO (concordance entre prétest et test). Il est seulement suspecté devant la constatation d’une HO déconnectée des symptômes ou si les symptômes ne sont pas évocateurs (discordance entre prétest et test) [1]. Il ne doit pas être écarté si une première recherche d’HO est négative et qu’une hypotension orthostatique reste vraisemblable ; il peut être utile de répéter les mesures de préférence le matin, une à deux heures après une prise médicamenteuse suspecte.
- Si la cause la plus fréquente de syncope chez les personnes âgées est l’hypotension posturale, la syncope a souvent plus d’une seule cause.
B – La recherche d’une hypersensibilité du sinus carotidien (SC)
La Société européenne de cardiologie recommande depuis de nombreuses années de rechercher comme cause de syncope une hypersensibilité du sinus carotidien [1]. En effet, avec l’âge et en particulier chez l’homme > 65 ans [13], on constate une hypersensibilité du sinus carotidien. Celle-ci est définie par « la survenue d’une pause ventriculaire de durée > 3 sec et/ou une chute de la tension artérielle systolique ≥ 50 mmHg » lors de la stimulation mécanique externe du baroréflexe carotidien (nerf sinusal de Hering situé dans l’adventice du bulbe carotidien, avant la division de la carotide primitive). Des stimuli (rotation brusque ou renversement en arrière de la tête, nœud de cravate, foulard ou chemise à col trop serré, rasage…) à l’origine de la syncope sont parfois identifiés par l’interrogatoire. La triade symptomatique complète, mais rarissime, comprend vertige, syncope et convulsions.
- Le massage sinocarotidien (MSC) est « indiqué chez les patients âgés de plus de 40 ans présentant une syncope d’origine inconnue, compatible avec un mécanisme réflexe » (classe IB) [1]. Ce geste peut être « réalisé si besoin dans l’évaluation initiale d’une syncope » [1] et donc au lit du patient en médecine d’urgence. La méthode est parfaitement décrite dans cette vidéo du New england journal of medicine [14]. Avant le MSC, le patient doit être informé du déroulement du geste et des renseignements attendus. Le patient doit être prévenu que le massage est un peu désagréable. Il doit être allongé de préférence avec la nuque en extension et l’activité électrique de son cœur doit être enregistrée tout au long de l’examen (monitorage scopique et ECG de préférence) [13][14]. Une mesure automatique continue de la tension artérielle peut être utile pour ne pas méconnaître une éventuelle réponse vasodépressive exclusive [13][14].
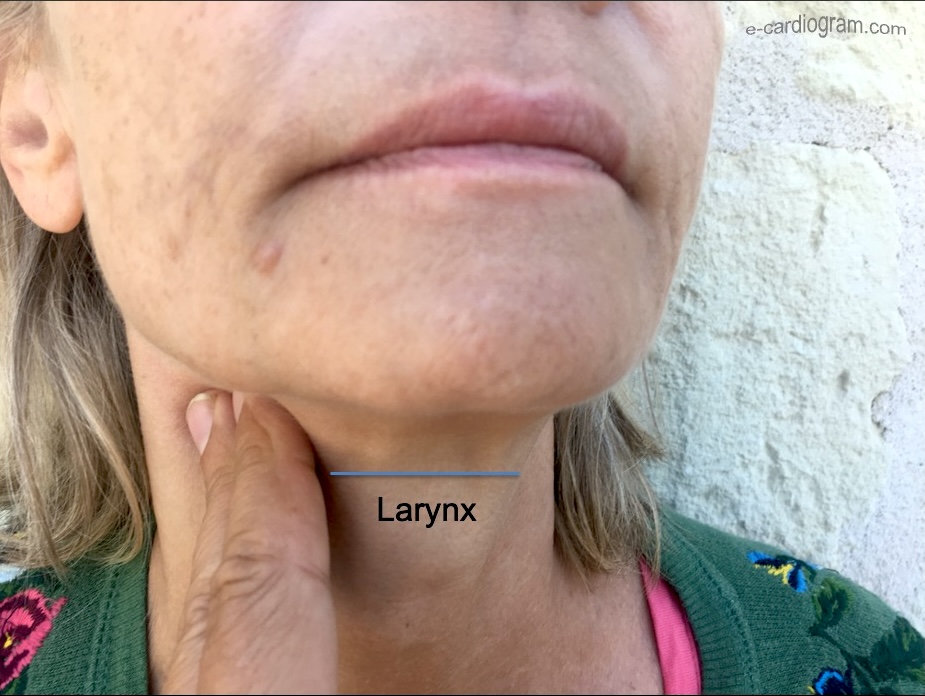 Le MSC s’effectue avec deux doigts (parfois le pouce) au niveau de la carotide sous-mandibulaire qui passe verticalement entre le muscle sterno-cléido-mastoïdien et le larynx (pomme d’Adam). La carotide est repérée par sa pulsatilité, au mieux après une légère rotation de la tête du patient du côté opposé au massage. Le massage débute par une pression bidigitale (index en haut, médius en bas) brève et légère (épreuve de Czennak) qui est souvent suffisante pour déclencher une stimulation nodo-frénatrice réflexe (inhibition parasympathique). Il se poursuit pendant 5-10 sec (13,14). Une réduction transitoire de la fréquence sinusale, un ralentissement de la conduction AV (l’intervalle PR s’allonge), une réduction de la taille des ondes P et une baisse légère de la tension artérielle peuvent survenir (14). Une asystolie transitoire (par suppression de l’automatisme sinusal ± bloc sinoatrial ± bloc atrioventriculaire) et donc une syncope peuvent survenir. Pour cette raison, il faut observer le patient et son activité électrique cardiaque. Si le massage d’une carotide est sans effet, il faut entreprendre le MSC de l’autre carotide (jamais simultanément) [1][14].
Le MSC s’effectue avec deux doigts (parfois le pouce) au niveau de la carotide sous-mandibulaire qui passe verticalement entre le muscle sterno-cléido-mastoïdien et le larynx (pomme d’Adam). La carotide est repérée par sa pulsatilité, au mieux après une légère rotation de la tête du patient du côté opposé au massage. Le massage débute par une pression bidigitale (index en haut, médius en bas) brève et légère (épreuve de Czennak) qui est souvent suffisante pour déclencher une stimulation nodo-frénatrice réflexe (inhibition parasympathique). Il se poursuit pendant 5-10 sec (13,14). Une réduction transitoire de la fréquence sinusale, un ralentissement de la conduction AV (l’intervalle PR s’allonge), une réduction de la taille des ondes P et une baisse légère de la tension artérielle peuvent survenir (14). Une asystolie transitoire (par suppression de l’automatisme sinusal ± bloc sinoatrial ± bloc atrioventriculaire) et donc une syncope peuvent survenir. Pour cette raison, il faut observer le patient et son activité électrique cardiaque. Si le massage d’une carotide est sans effet, il faut entreprendre le MSC de l’autre carotide (jamais simultanément) [1][14].
- Bien que les complications neurologiques soient très rares, « le risque de provocation d’un accident ischémique transitoire après MSC suggère que celui-ci doit être pratiqué avec précaution chez un patient qui a déjà eu un accident ischémique transitoire, un accident vasculaire cérébral ou qui présente une sténose carotidienne > 70% ». En effet, le risque de “décrocher” une plaque athéromateuse au cours du MSC et de provoquer une embolie cérébrale est vraisemblablement plus fréquent chez ces patients. Réaliser avant le massage une échographie-Doppler par un spécialiste n’est pas strictement recommandé, mais il paraît prudent de vérifier chacune des carotides au point de massage par une échographie clinique [14]. De même, est-il logiquement prudent d’éviter chez les sujets coronariens de provoquer des pauses ventriculaires qui durent en moyenne 7,6 ± 2,2 sec et s’accompagnent de chute tensionnelle [13].
- En cas de risque/bénéfice incertain, il me semble préférable de surseoir à la réalisation de ce geste en médecine d’urgence. On peut alors envisager de le remplacer par une manœuvre de Valsalva éclair (toux) ou écourté. La manœuvre de Valsalva est également recommandée pour le diagnostic de certaines formes HO (neurogène) et de syncope réflexe (toux, rire, éternuement, haltérophilie) [1].
Le diagnostic d’une « hypersensibilité du SC » est posé lorsque le massage de l’un ou l’autre SC provoque une bradycardie avec pause ventriculaire > 3 sec (asystolie) et/ou une hypotension ≥ 50 mmHg [1][14]. Le diagnostic de « syndrome du SC » est posé lorsque le massage du SC reproduit les symptômes spontanés du patient, et que le patient présente des caractéristiques cliniques compatibles avec un mécanisme réflexe de syncope (classe IB) [1]. Dans cette population, la prévalence du syndrome du SC est de 8,8% [13]. L’hypersensibilité du sinus carotidien est fréquente chez les patients âgés et par conséquent peut être découverte fortuitement chez les patients qui présentent un autre mécanisme de syncope. Un MSC négatif en position couchée n’élimine pas le diagnostic d’hypersensibilité du SC, car la méthode complète de dépistage inclut un MSC couché puis debout.
Autres examens
Ils sont généralement programmés en unité d’exploration fonctionnelle. Test d’inclinaison (tilt test, réf 2023 [19]), enregistrement longue durée de l’activité électrique du cœur ou de la tension artérielle [26], interrogation du pacemaker/défibrillateur (interrogation par le spécialiste de l’activité cardiaque mémorisée), épreuve d’effort, test à l’adénosine pour rechercher une dysfonction sinusale, évaluation neurologique à la recherche d’une dysautonomie, électroencéphalogramme…
Des examens plus invasifs peuvent être nécessaires. Les recommandations 2018 accordent une grande place aux enregistreurs ECG implantables, recommandés quand il semble exister un risque de mort subite, mais insuffisant pour l’implantation d’emblée d’un défibrillateur, chez les patients suspects de syncope d’origine arythmique ou en cas de syncopes récidivantes responsables de traumatismes sévères (cf. Holter implantable).
Prise en charge hospitalière ?
Recommandations ESC 2018
Elles proposent des algorithmes décisionnels pertinents qui permettent de distinguer trois profils de patients [1] :
- les patients suspects de syncope d’origine vagale, qui, après évaluation initiale, ne nécessitent pas d’exploration complémentaire. Ils peuvent rapidement sortir de l’hôpital et représentent environ la moitié des cas ;
- les patients présentant un risque vital lié à une cardiopathie ou une anomalie ECG. Ces patients, environ 10 % des admissions, sont monitorés (scope/télémétrie) et hospitalisés d’emblée ;
- les patients qui nécessitent d’être explorés au-delà de l’évaluation initiale, mais chez qui les examens peuvent être différés et programmés en ambulatoire ou en unité d’hospitalisation des urgences.
Raisonnement Bayesien
La « logique Bayesienne » qui combine une estimation prétest de risque/pronostic à court terme avec les résultats d’un test ou les algorithmes proposés par la Société européenne de cardiologie, facilite la prise de décision qui se résume schématiquement en trois choix :
1. Abstention dans la poursuite des investigations (risque faible) ; le diagnostic de syncope réflexe ou hypotension orthostatique est hautement probable, l’examen clinique ou l’électrocardiogramme sont normaux et le risque de récurrences à court terme est peu probable –> le patient peut quitter la structure d’urgence avec l’information liée au diagnostic et les conseils d’usage (si les facteurs déclenchants peuvent être corrigés et/ou enseignés).
2. Indécision avec poursuite des investigations (risque ni faible ni fort) ; le mécanisme de la perte de connaissance est incertain, le risque de récurrence à court terme est envisageable –> le patient peut bénéficier d’une admission de courte durée en structure d’urgence ou en unité ambulatoire spécialisée dans la prise en charge des syncopes. L’avis d’un expert, un monitorage ou des examens complémentaires sont généralement utiles.
3. Décision d’une intervention (risque fort) ; le diagnostic de syncope cardiaque est hautement probable, le risque de récurrence à court terme est hautement probable –> le patient doit être hospitalisé en vue d’une approche diagnostique intensive ou un traitement spécifique urgent. Un monitorage avec possibilité de réanimation cardio-pulmonaire est recommandé.
D’autres critères interviennent dans la décision d’une prise en charge hospitalière plutôt qu’ambulatoire en l’absence de risque fort comme l’existence d’un traumatisme secondaire à la syncope, de syncopes répétées, de facteurs favorisants ou de comorbidité associée justifiant en soi une hospitalisation, ou une impossibilité de surveillance, de respecter les précautions à prendre ou de réaliser des investigations en ambulatoire.
Des scores pronostiques peuvent être utiles (voir diapo ESC 2018 [1]), mais semblent aussi performants qu’un praticien expérimenté [23]. Ils limitent l’utilisation des ressources inutiles (ex. complémentaires et hospitalisation, voir revue 2014 [21]: Tableau II : principaux scores de stratification du risque dans la syncope).

Si vous souhaitez améliorer ce contenu, merci de me contacter
Références. Réservées aux abonnés
La suite est réservée aux membres et stagiaires du site.
Se connecter | Devenir membre | Devenir stagiaire
La suite est réservée aux membres et stagiaires du site.
Se connecter | Devenir membre | Devenir stagiaire