Mort naturelle définie ainsi par l’ESC en 2015 [1].
Mort subite. « Événement mortel inattendu, non traumatique, survenant dans l’heure qui suit l’apparition des symptômes chez un sujet apparemment sain ». Sont incluses les hémorragies cérébrales et les embolies pulmonaires. Les étiologies cardio-vasculaires, et en particulier les infarctus, représentent environ 50% des causes, ce qui explique une prise en charge spécifique et une stratégie concertée autour de l’angiographie coronaire en extrême urgence (ESC 2024 [13]).
Mort subite cardiaque. « Décès par arrêt circulatoire inattendu, généralement dû à une arythmie cardiaque survenant dans l’heure suivant l’apparition des symptômes.
Arrêt cardiaque soudain. Décès suite à un arrêt circulatoire inattendu, généralement dû à une arythmie cardiaque survenant dans l’heure suivant l’apparition des symptômes, chez lequel une intervention médicale (par exemple, défibrillation) inverse l’événement.
Chez l’adulte, l’incidence annuelle chez l’adulte est estimée aux USA entre 1 et 2‰ par an [11]. En Europe, l’incidence moyennée de mort subite dans quatre registres nationaux entre 2012 et 2017 varie entre 0,37 et 0,40 ‰ [12].*
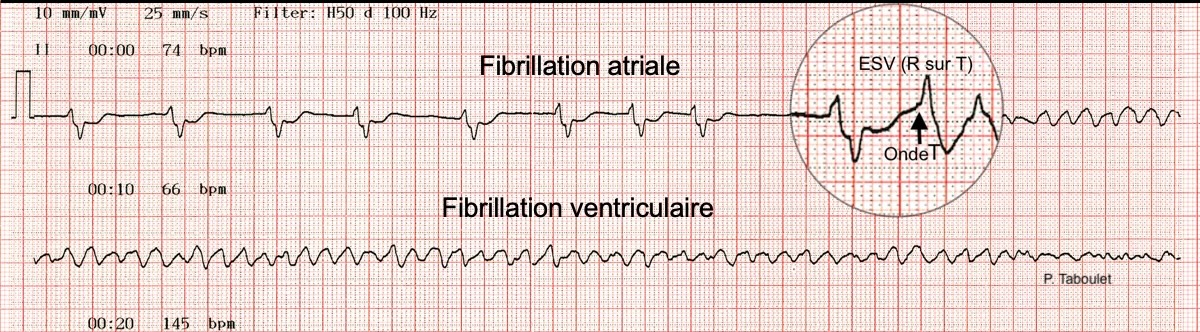
A – Fibrillation ventriculaire
La cause est le plus souvent une fibrillation ventriculaire inaugurale ou consécutive à un trouble du rythme sévère (ex. TV, torsade de pointes, FA préexcitée, pause ventriculaire…). En France, 50.000 patients décèdent de FV chaque année, âge moyen 65 ans (400 nourrissons, 500 sportifs), dont 80% à domicile (cf. MORT en DIRECT ?).
La mort subite frappe des sujets au repos ou pendant leur sommeil dans 44 % des cas, pendant un effort dans 15 % des cas, pendant des activités quotidiennes banales dans 37 % des cas, sur le lieu de travail dans 2 % des cas [Haissaguère 2015]. On comprend ainsi la place de la défibrillation précoce et le rôle joué par les défibrillateurs chez les sujets à risque [11].
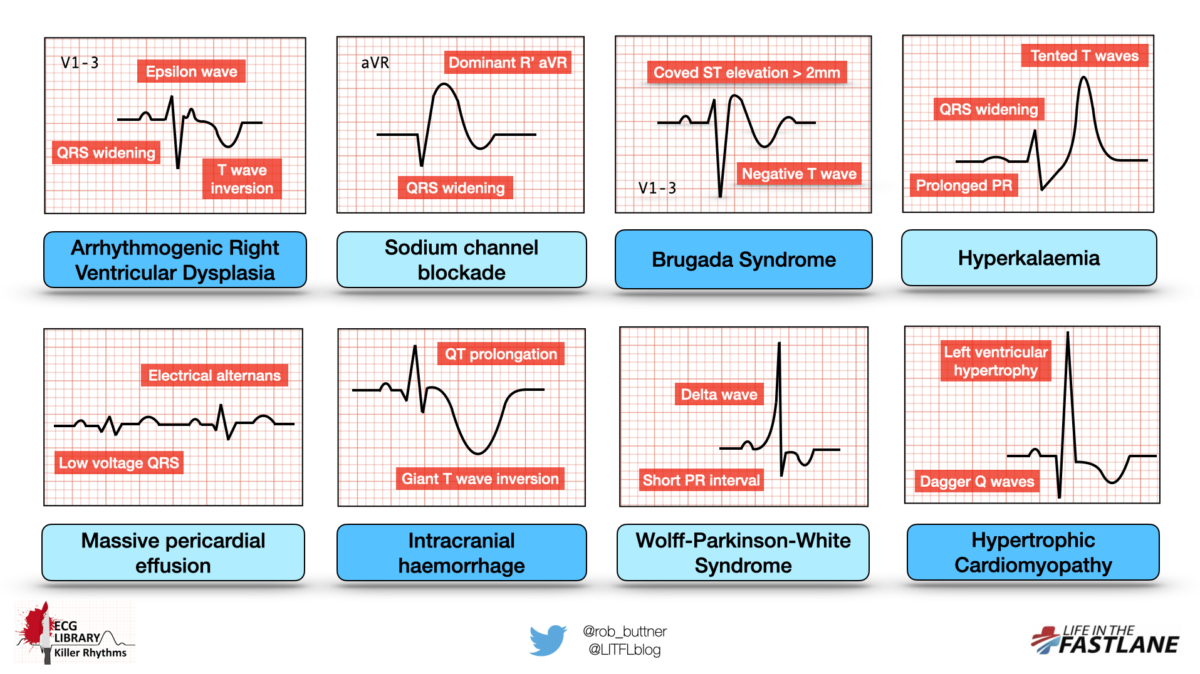
Les mécanismes arythmogènes sont majoritairement une réentrée ou un automatisme anormal (ESC 2017 [1bis]). Les substrats arythmogènes les plus fréquents sont les cardiopathies ischémiques et les anomalies de l’électrogénèse (cf. syndrome du QT long, syndrome de Brugada, syndrome de repolarisation précoce maligne, TV catécholergique, syndrome du QT court, FV idiopathique) [2], plus rarement les cardiomyopathies [8]. Une commotion cardiaque sans contusion peut déclencher exceptionnellement une FV (cf. Commotio cordis).
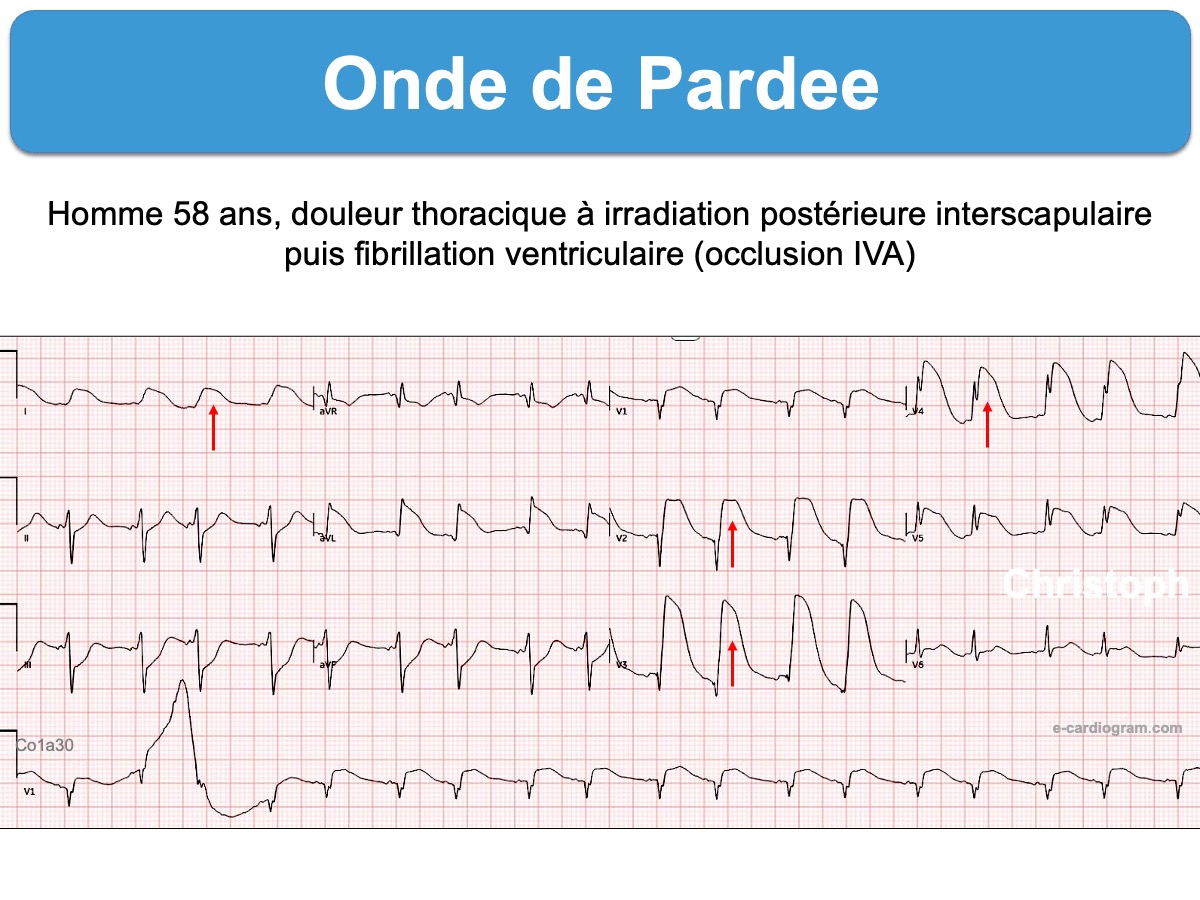
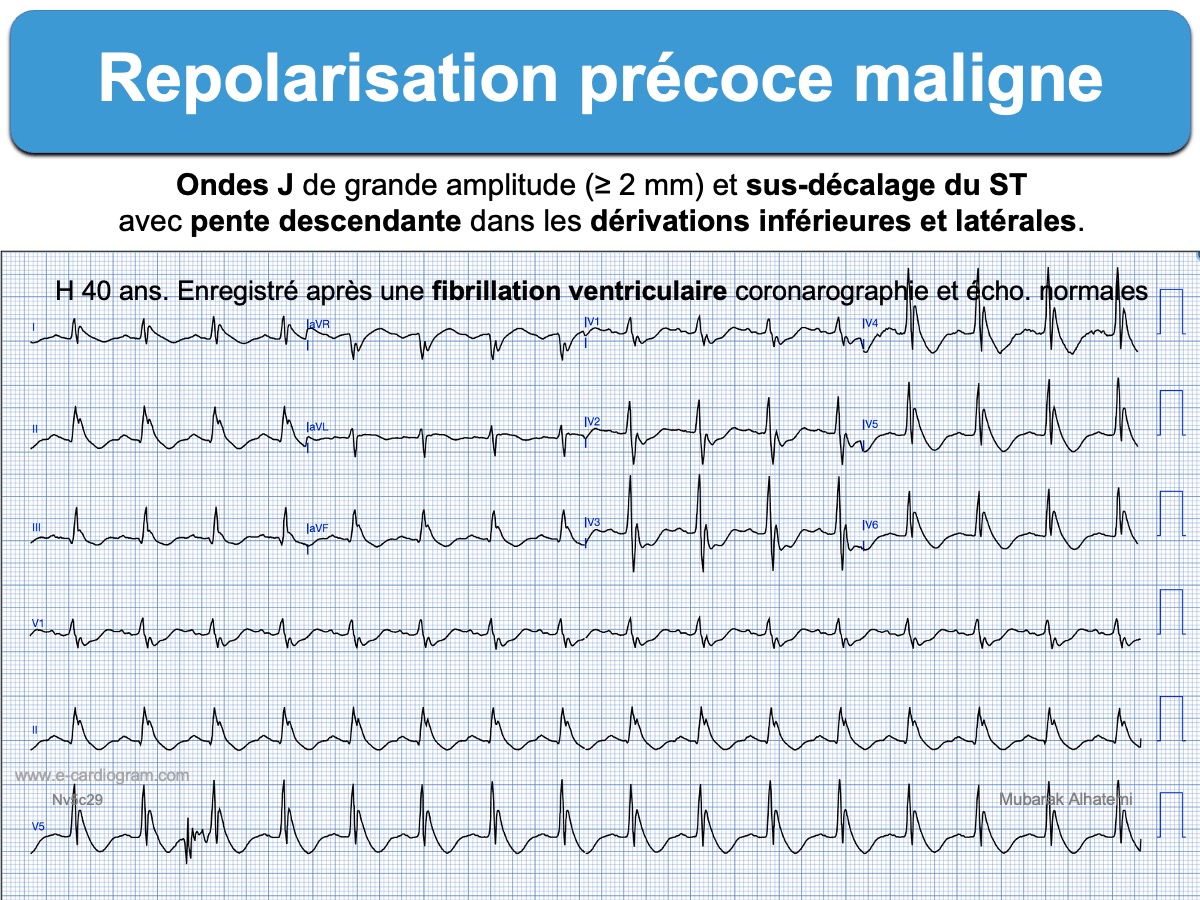
L’enregistrement immédiat de l’ECG après ressuscitation peut orienter vers une pathologie précise. Ci-dessous deux exemples : une occlusion coronaire aigüe (fréquente) et d’une repolarisation précoce maligne (rarissime).
Les facteurs initiant sont par exemple une ischémie myocardique ou une hypoxie, une hypertonie vagale, un stress ou un effort (catécholamines), une perturbation métabolique (ex. hypokaliémie, hypothermie), un médicament (ex. cocaïne) ou un toxique.
Coronary artery disease is the predominant cause of sudden cardiac death in older persons, whereas among persons 1 to 35 years of age, sudden cardiac death is more often caused by structural heart disease, including hypertrophic cardiomyopathy, dilated cardiomyopathy, arrhythmogenic right ventricular cardiomyopathy, myocarditis, and primary arrhythmogenic disorders (such as the congenital long-QT syndrome, the Brugada syndrome, and catecholaminergic polymorphic ventricular tachycardia). Many of these cardiac causes of sudden cardiac death among children and young adults have an underlying genetic basis
De nombreuses techniques pour la stratification du risque ont été mises au point pour détecter la présence d’anomalies de la conduction et de la repolarisation ventriculaire à l’origine d’une rentrée ou d’un substrat arythmogène ou d’un facteur gâchette à l’origine d’une automaticité anormale en fonction de la pathologie somatique ou dans une population générale [3][4]. Certaines reposent simplement sur la lecture de l’ECG [5][6]. D’autres techniques sont en cours de développement pour la stratification du risque en cas de coronaropathie [7][10][13]. Ces techniques ont fait l’objet d’une évaluation en 2014 [8] et de recommandations ESC en 2015 [9] et 2024 [13].
B – ASYSTOLE
L’arrêt de l’activité électrique du cœur survient plus ou moins brutalement au cours de l’évolution d’une cardiopathie sévère ou d’une défaillance secondaire de la pompe cardiaque (embolie pulmonaire, dissection aortique, tamponnade, hyperkaliémie, anoxie, choc septique, intoxication avec effet stabilisant de membrane…).
TESTEZ VOUS
- Lire la diapo ci-dessus puis faire cet exercice (fast in the fast lane)
- Cardiocases Masterclass on line
Biblio actualisée automatiquement Pubmed ici
Références (réservées aux abonnés)
La suite est réservée aux membres et stagiaires du site.
Se connecter | Devenir membre | Devenir stagiaire