L’ECG est la pierre angulaire de l’identification et la classification des SCA. Sa réalisation en cas de douleur thoracique ou de tout autre symptôme évocateur d’infarctus doit être la plus rapide possible, au mieux dans les 10 minutes après le premier examen médical, avant les résultats de tests biologiques et sous surveillance médicale constante (ESC 2023 [1]). Si le patient consulte aux Urgences, l’ECG doit être réalisé lors du triage par un(e) infirmier(e) parfaitement formé(e) à la reconnaissance des symptômes évocateurs d’infarctus et aux pièges [2]. Si l’on pense qu’un patient fait un SCA, prescrire un dosage de troponine pour guider la réalisation éventuelle d’un électrocardiogramme est une faute, qui peut retarder le diagnostic d’infarctus et conduire à un préjudice…
Le bon étalonnage de l’appareil ECG doit être vérifié (25 mm/sec et 1 mm = 0,1 mV) et le choix des filtres adaptés à la qualité du tracé (recommandés : passe-bas > 0,05-0,67 Hz et passe-haut ≤ 150 Hz). La ligne de base doit être stable pour ne pas gêner la lecture des segments PR ou ST. Pour supprimer les artéfacts de haute fréquence, un réglage du filtre passe-haut ≤ 100 voire ≤ 35 Hz ou un positionnement plus proximal des électrodes des membres supérieurs (milieu du bras, latéralement sous le deltoïde) et inférieurs (crête iliaque antérosupérieure ou bas abdomen, électrodes séparées de 10 cm) en cas de tremblements peut être utile au risque d’atténuer certaines anomalies d’origine ischémique (ondes Q, QRS fragmentés) [3].
Valeur diagnostique et attitude pratique
En cas de douleur thoracique ou de tout autre symptôme évocateur d’infarctus, l’ECG initial révèle dans un faible pourcentage de cas (< 20%) des anomalies compatibles avec un syndrome coronaire aigu (SCA). La stratégie de prise en charge initiale dépend en première intention de l’existence ou non d’un sus-décalage de ST (ST+) –> SCA avec sus-décalage de ST.
Les seuils d’élévation du point J qui définissent un SCA ST+ sont universellement acceptés (cf. Point J, ESC 2018 [5]). Néanmoins, si ces seuils « universels » sont bien corrélés avec l’existence d’une occlusion coronaire aiguë, environ 30 % des occlusions/subocclusions échappent à la tyrannie du ST+ académique et se présentent sous des formes variées qui font de l’ECG un outil parfois complexe pour guider la thérapeutique initiale (OMI Manifesto de S. Smith avril 2018).
Ainsi la prise en charge médicale initiale ne dépend pas que de l’existence ou non d’un ST+ académique sur l’ECG, mais aussi de la datation précise des symptômes, de la connaissance du terrain (antécédent, médicaments…), d’une bonne connaissance des formes subtiles d’occlusion coronaire aiguë, de la recherche d’une forme instable (douleur persistante ≥ 2 heures, instabilité hémodynamique, arythmie ventriculaire), des ECG répétés (disparition ou apparition d’une onde T+, d’un ST+ ou de QRS modifiés par l’ischémie), de la cinétique de la troponine –> cf. SCA avec équivalent ST+.
En cas d’anomalie évocatrice d’infarctus ST+ ou d’ischémie myocardique, il faut monitorer le patient (scope) et analyser parfaitement le rythme, la conduction (atrioventriculaire et intraventriculaire), les complexes QRS (cf. Complexes QRS modifiés par l’ischémie), puis le segment ST (cf. Sus-décalage de ST, onde de Pardee, sous-décalage de ST…), les ondes T (cf. ondes T amples ischémiques, onde T de reperfusion) et enfin l’intervalle QT qui s’allonge parfois en cas d’ischémie.
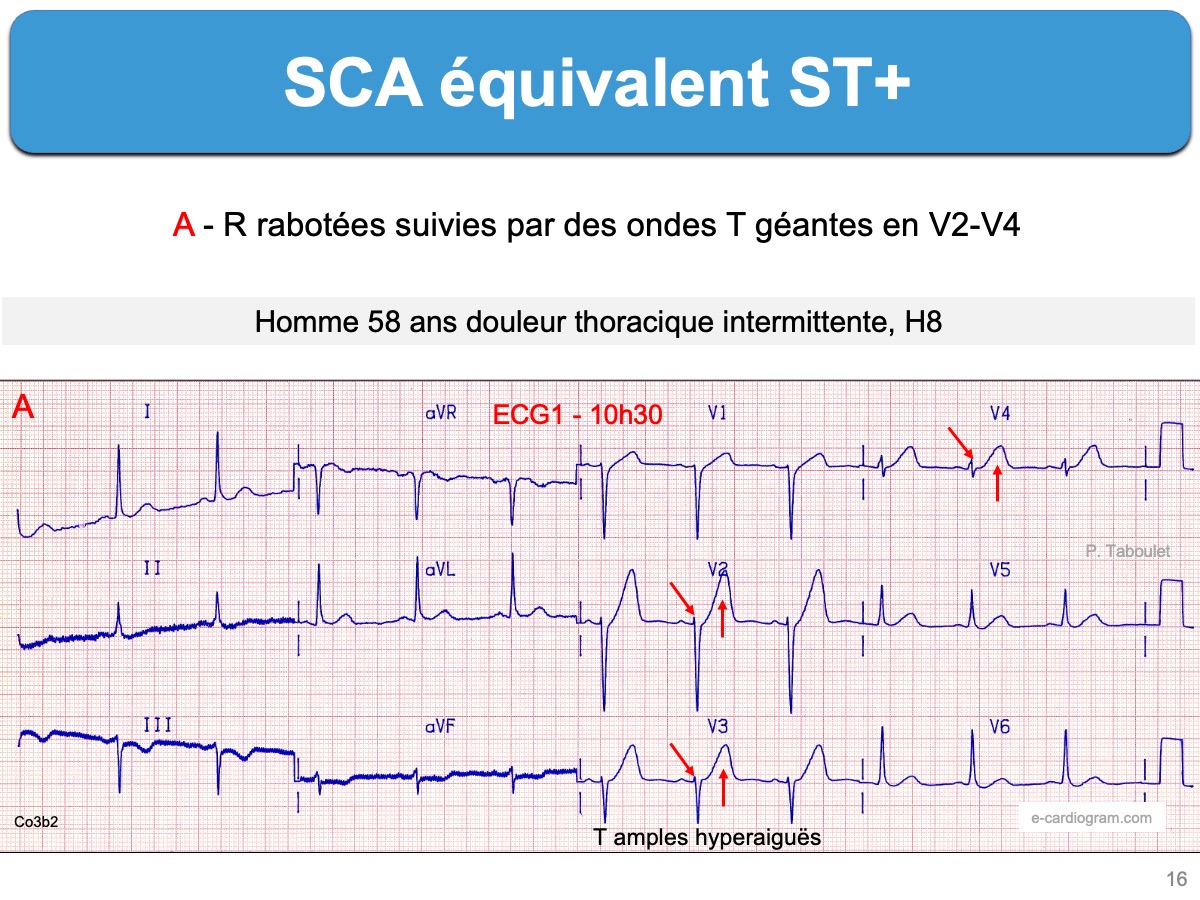
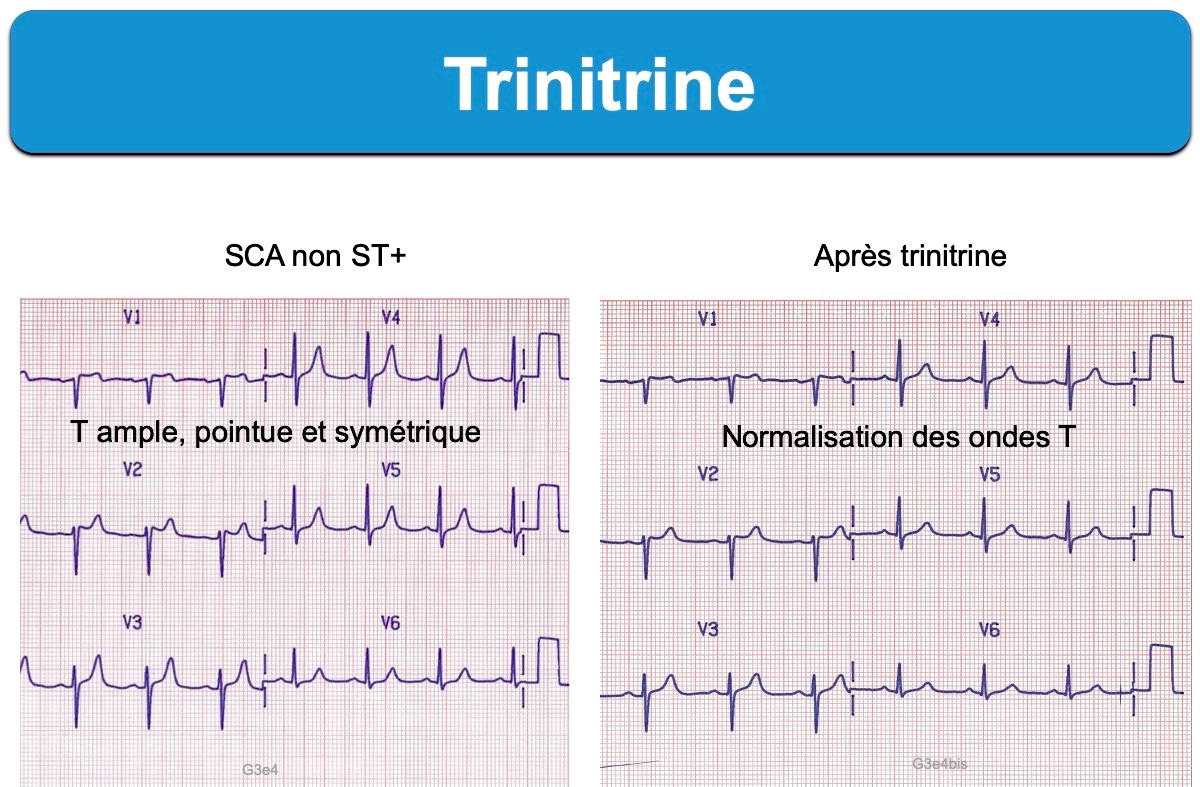
L’exemple ci-dessous illustre l’évolution en 40 minutes d’un SCA non ST+ (ondes T géantes hyperaiguës) vers un SCA ST+.
Ci-dessous : Ondes T amples ischémiques aiguës en territoire inférieur évoluant rapidement vers un aspect d‘infarctus ST+

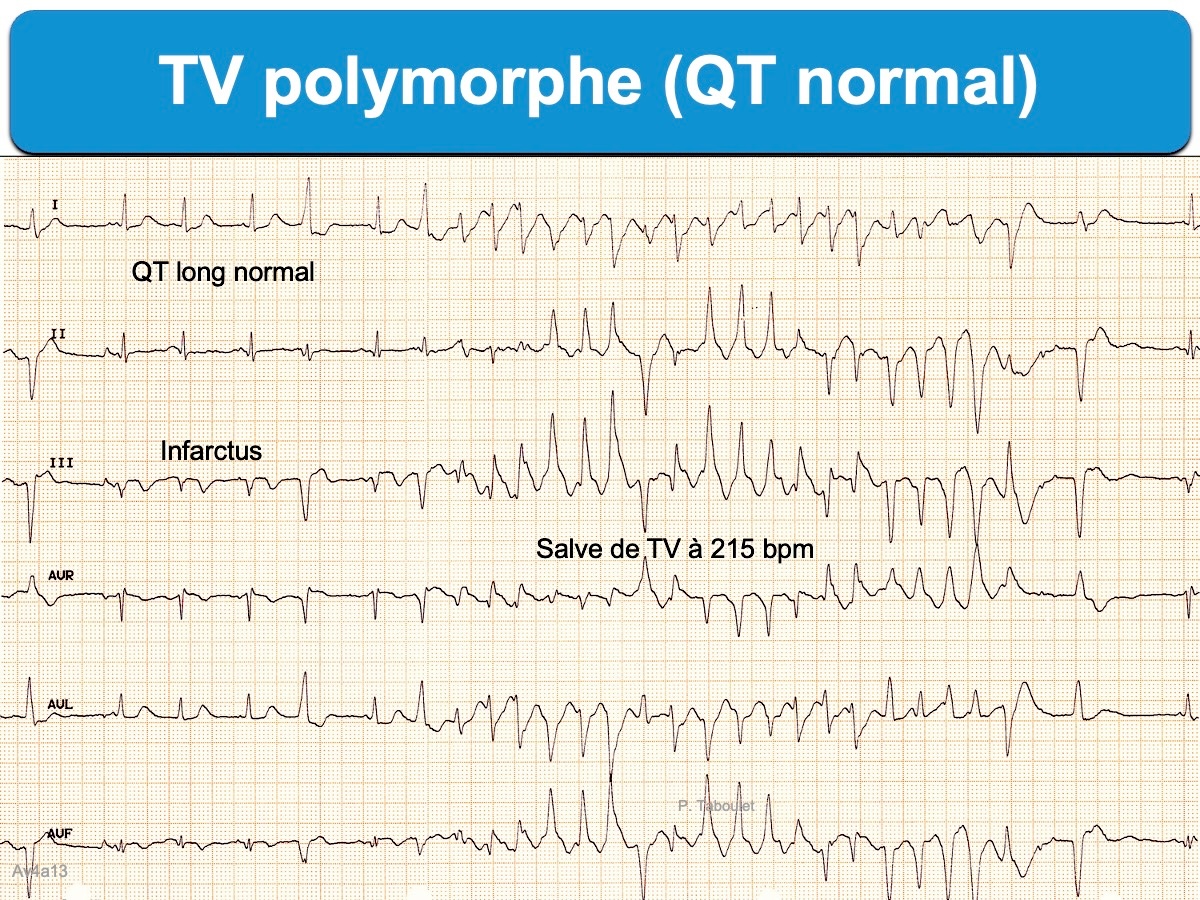
Si la suspicion d’infarctus est forte, en particulier devant l’existence d’extrasystoles ventriculaires, l’installation ou le transport du patient doit se faire en présence d’un défibrillateur opérationnel, car le tracé peut évoluer rapidement vers une tachycardie ventriculaire polymorphe ou une fibrillation ventriculaire.
De très nombreux ECG sont difficiles à interpréter et une grande compétence est nécessaire pour reconnaitre les infarctus par occlusion coronaire aiguë sans sus-décalage de ST (appelé en anglais « OMI non STEMI » pour occlusion myocardial infarction sans élévation de ST).
Ce n’est pas l’ECG qui n’est pas spécifique, c’est le médecin (Steve Smith).
Voici un résumé de la classification ECG des SCA en sept 2025

Il est indispensable de se former aux petits signes d’occlusion coronaire (cf. SCA sans sus-décalage de ST) avant de dire qu’un ECG est normal/non spécifique ou de perdre du temps et le muscle du malade (« time is muscle« ) avec des dosages itératifs de troponine, quand le diagnostic d’occlusion coronaire aigu est évident (malgré l’absence de ST+ académique) et que les symptômes angineux perdurent (cf. SCA équivalent ST+).
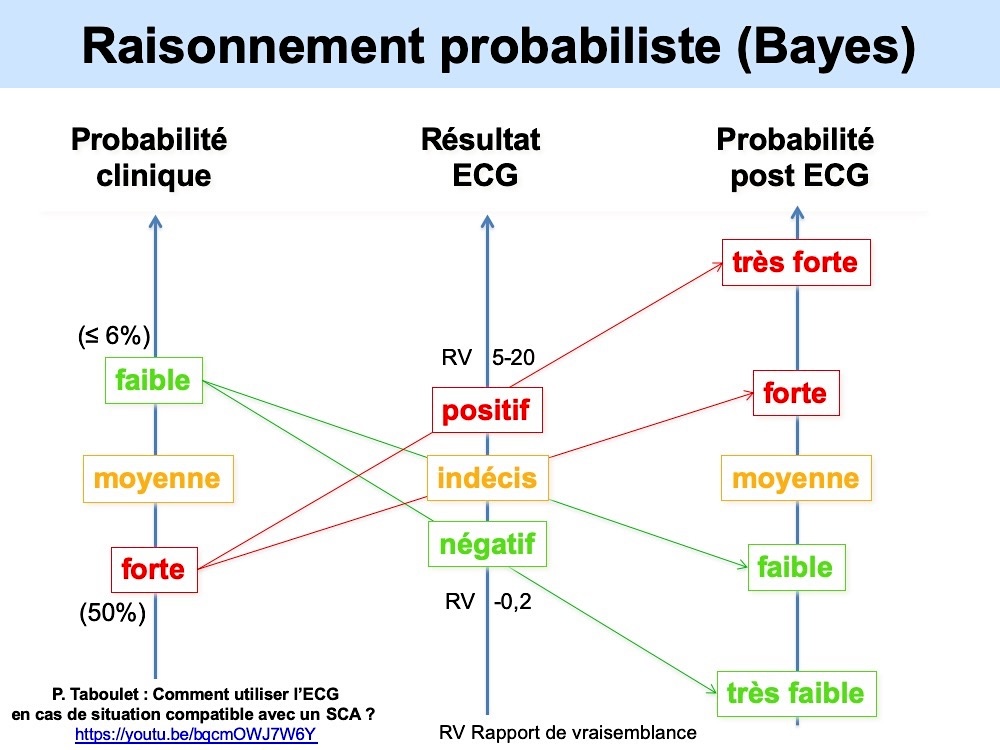
Enfin, l’ECG est un test qui s’inscrit dans une démarche Bayesienne qui implique une estimation de la probabilité prétest d’infarctus (ex-faible, moyenne, forte) et une combinaison avec les résultats (+, -, 0) du test pour obtenir une probabilité post-test (ex. très faible, faible, moyenne, forte, très forte), et en fonction décider d’une abstention (évaluation d’autres diagnostics), d’une intervention ou rester dans l’indécision (autres tests) (Lire [27]).
 Vidéo YouTube PT (2014, 25 min) : ECG au cours du SCA (raisonnement bayesien).
Vidéo YouTube PT (2014, 25 min) : ECG au cours du SCA (raisonnement bayesien).
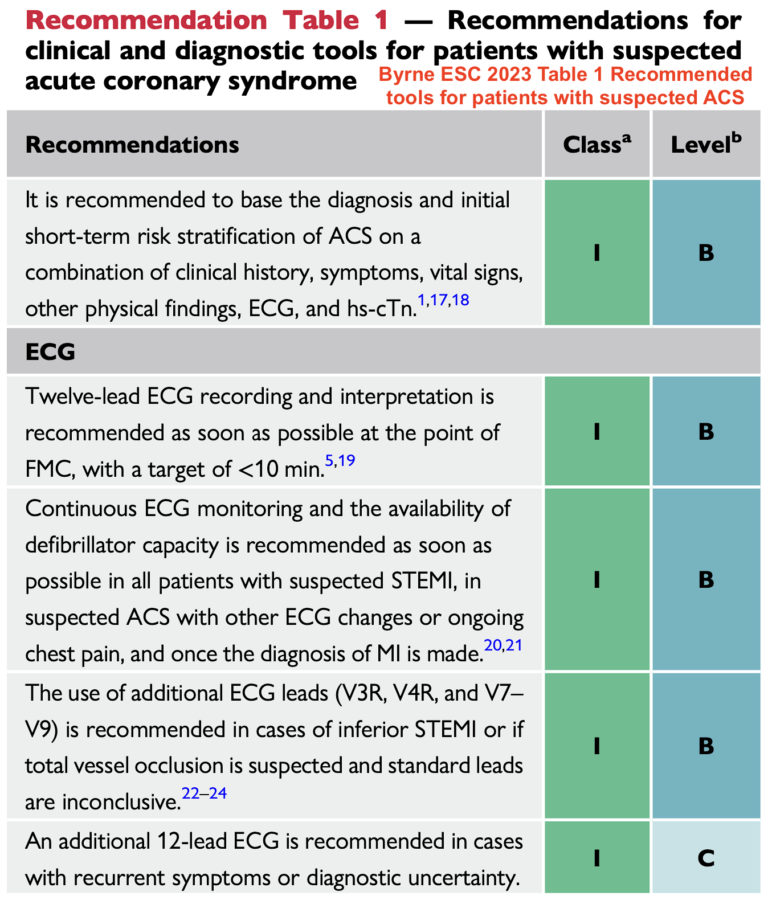
L’enregistrement des 18 dérivations. Les auteurs des recommandations de l’ESC 2018 [5], puis 2003 [1] précisent que les dérivations additionnelles (V3R, V4R, V7-V9) ne sont pas recommandées en routine.
L’enregistrement précoce des dérivations précordiales droites V3R-V4R (qui explorent le territoire du ventricule droit) est recommandé en cas d’infarctus dans le territoire inférieur si une extension au ventricule droit est « suspectée devant un sus-décalage de ST ≥ 1 mm en V1 ou VR » (ou ST+ plus ample en V1 qu’en V2) (cf. Infarctus du ventricule droit) [8]. L’infarctus du VD est alors retenu devant un ST+ ≥ 0,5 mm en V3R-V4R (≥ 1 mm chez les hommes < 30 ans). Ce sus-décalage peut être transitoire et « l’absence de sus-décalage de ST en territoire V3R-V4R n’exclut pas l’infarctus du VD » [5].
L’enregistrement précoce des précordiales postérieures V7-V9 est « fortement » recommandé en cas d’infarctus dans le territoire inférieur ou de « suspicion clinique forte d’occlusion coronaire (circonflexe) avec ECG initial non-concluant » ou « en cas de sous-décalage de ST en dérivations V1-V3 et tout particulièrement si la portion terminale de l’onde T est positive » [5]; il faut alors rechercher un infarctus au territoire inférobasal si ST+ ≥ 0,5 mm (≥ 1 mm chez les hommes < 40 ans) (cf. Infarctus basal). Cet infarctus est généralement concomitant d’un infarctus dans le territoire inférieur (infarctus inférobasal), mais il peut être isolé [5].
L’hypothèse ischémique ne peut être éliminée
Si le patient reste symptomatique, l’ECG devra être renouvelé toutes les 15-30 minutes et le monitorage (scope) sera poursuivi jusqu’au résultat des tests biologiques et l’orientation finale [5]. Les électrodes seront laissées en place jusqu’à la fin de la démarche diagnostique (ou leur emplacement sera marqué sur le thorax) pour mieux comparer les ECG successifs et l’enregistrement initial sera comparé tant que faire se peut avec un ECG de référence. De petites modifications et le moindre ST+ doivent renforcer l’hypothèse d’une occlusion coronaire.
L’apparition de modifications ECG spontanément ou après un test à la trinitrine, par rapport à un tracé de référence ou sur une série de tracés est prédictive d’un SCA (Voir cas clinique LITFL cas 125).
Si le patient est ou devient asymptomatique, l’ECG pourra être répété de façon plus espacée (sauf en cas de récidive douloureuse) en attendant le résultat des marqueurs biologiques (la stratégie de dosage de la troponine en point of care à H0 et H2 semble la plus pertinente [28]). En aucun cas, le dosage de la troponine ne doit dispenser de réaliser en premier un électrocardiogramme… et de réitérer de façon rapprochée (ex 15 min).
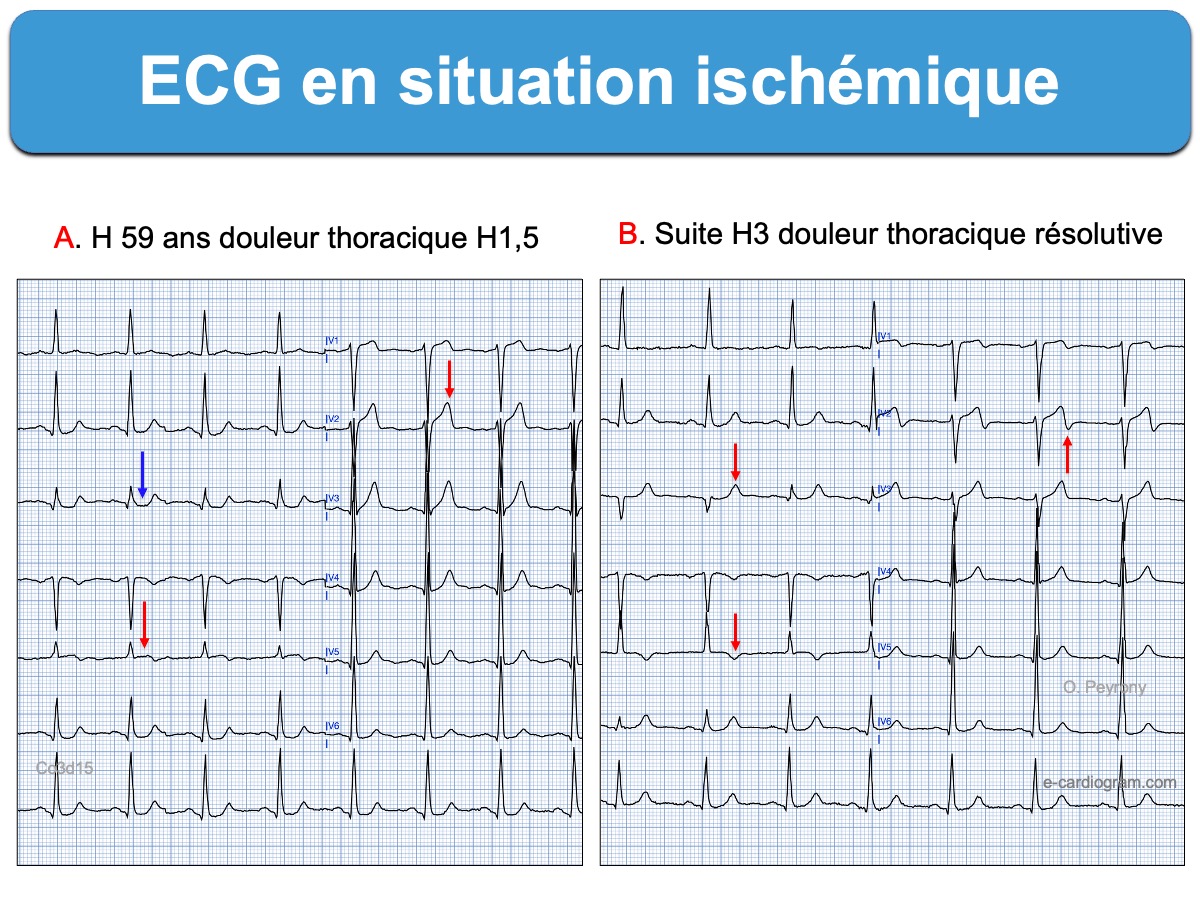
Ci dessous. H59 ans ECG per critique puis après résolution de la douleur. Les signes de reperfusion coronaire sont caractéristiques.
Un ECG normal (ou qui paraît normal) chez un patient souffrant de douleurs thoraciques n’exclut pas la possibilité de SCA : 1% à 6% de ces patients ont une occlusion coronaire aiguë non décelable par l’ECG, et au moins 4% ont un angor instable [11]. Un dosage de troponine doit être le plus précoce possible. Un ECG normal et des marqueurs biologiques normaux et répétés éliminent un infarctus, mais pas une insuffisance coronaire [12].
Toute douleur thoracique évocatrice d’un SCA, persistante ou récurrente malgré un traitement médical, avec un ou des ECG normaux ou non concluants (et une troponine positive) peut être une occlusion coronaire aiguë +++. Aussi est-il recommandé de proposer le patient pour une stratégie invasive comprenant une angiographie coronaire (ESC 2023 [1]).
Homme 69 ans. Douleur dorsale tenace depuis 24h. Troponine 10.000 ! Occlusion circonflexe et sténose IVA 70%

Compétence des médecins pour reconnaitre des signes ECG d’infarctus (Réf. P. Taboulet. 100 ECG autour de l’infarctus. S–éditions 2020)
- Lors de tests (série d’ECG consécutifs proposés hors vie réelle), les évaluations de performance des médecins à reconnaître des signes ECG de SCA ST+ sont décevantes, voire inquiétantes, même si la méthodologie utilisée est parfois/souvent discutable. La sensibilité mesurée est proche de 2/3 au pire et une spécificité proche de 4/5 au mieux [13][14][15]. Les cardiologues expérimentés ne font guère mieux [16].
- Dans la vie réelle, la non-reconnaissance d’un infarctus ST+ (faux négatifs) varie entre 5,9% [17] et 29% [18] et le non-diagnostic de cœur ischémique avec non-admission survient dans environ 2% des cas et aggrave le pronostic [19][20][21]. Les faux positifs de ST+ sont aussi voire plus nombreux (cf. Diagnostics différentiels). Les conséquences sont par exemple une thrombolyse/anticoagulation inutile ou un transport inutile en salle de cathétérisation, estimés à 10% aux USA [22][23][24][25].
Pourquoi le diagnostic ECG d’infarctus est difficile ?
La technique d’enregistrement est mauvaise
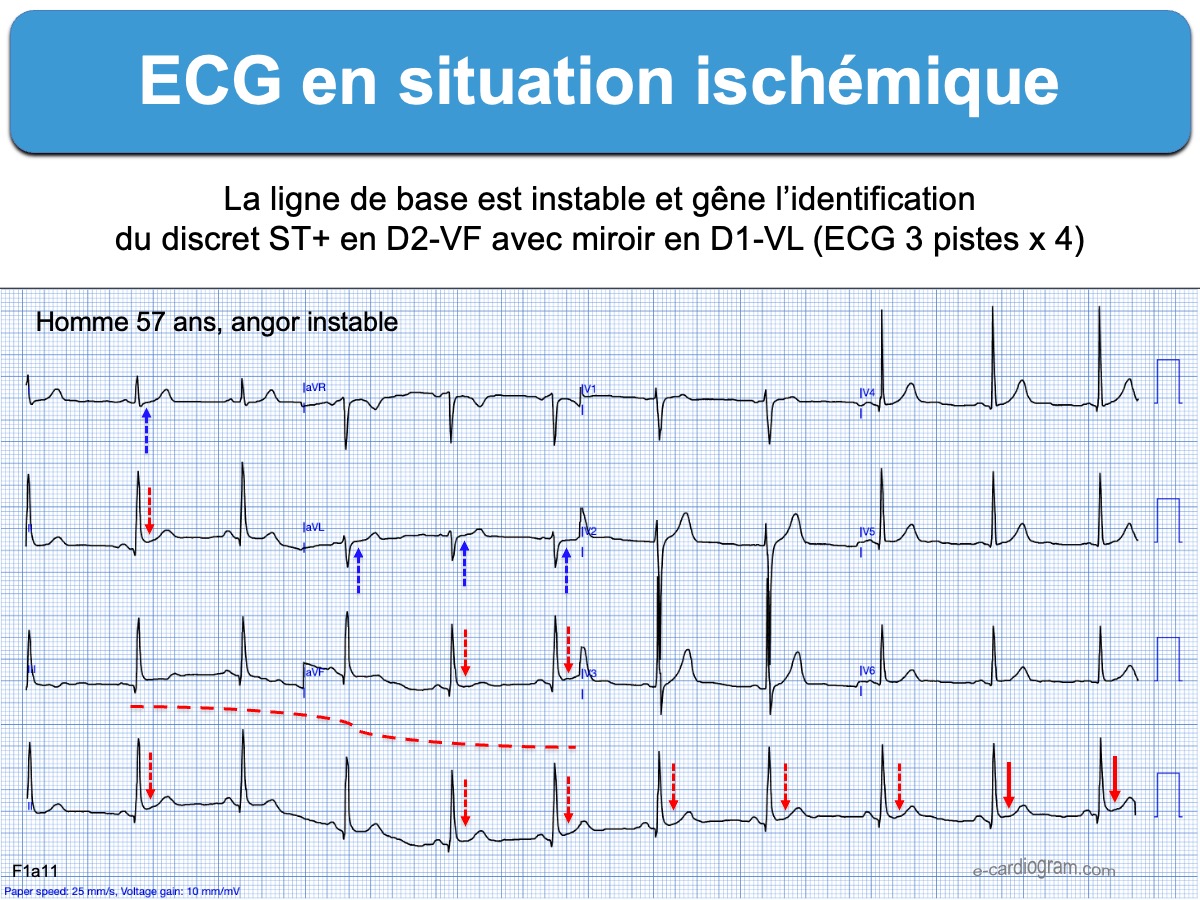
- L’ECG est peu lisible en raison d’un enregistrement de mauvaise qualité (tremblements, artéfacts, ECG 3 x 4 pistes), une erreur d’étalonnage, un mauvais réglage des filtres, un mauvais positionnement des électrodes…
Le niveau de connaissance/expérience est insuffisant
- Le sus-décalage de ST est subtil (< seuil académique) ou limité à une seule dérivation qui n’a qu’une seule dérivation contiguë (ex. en D3, VL, VR ou V1) ou son miroir n’est pas identifié (cf. Infarctus sans sus-décalage de ST+).
F 47 ans, douleur thoracique évocatrice de SCA. ECG considéré comme normal. Peut-on utiliser l’ECG comme un « rule out test » ?

Réponse: NON. Le sus-décalage de ST est subtil en D3 car les QRS sont microvoltés, mais le miroir ST- en VL ne vous a pas échappé… Dissection spontanée de la CD. Heureusement, la troponine a été dosée et le diagnostic d’infarctus assuré.
- Des complexes QRS larges compliquent l’interprétation de la repolarisation et la règle de la discordance appropriée n’est pas connue (cf. Infarctus avec QRS larges).
- Le sous-décalage de ST est interprété à tort comme une anomalie secondaire de la repolarisation, malgré un pattern typique « équivalent ST+ » d’occlusion coronaire (cf. Infarctus équivalent ST+).
- Les ondes T amples (qui dépassent R dans au moins deux dérivations contiguës) ne sont pas toujours faciles à reconnaitre.
- Des petites anomalies combinées des QRS, du ST, de l’onde T ou de l’onde U évocatrices d’ischémie ne sont pas identifiées (cf. Infarctus non ST+) [32].
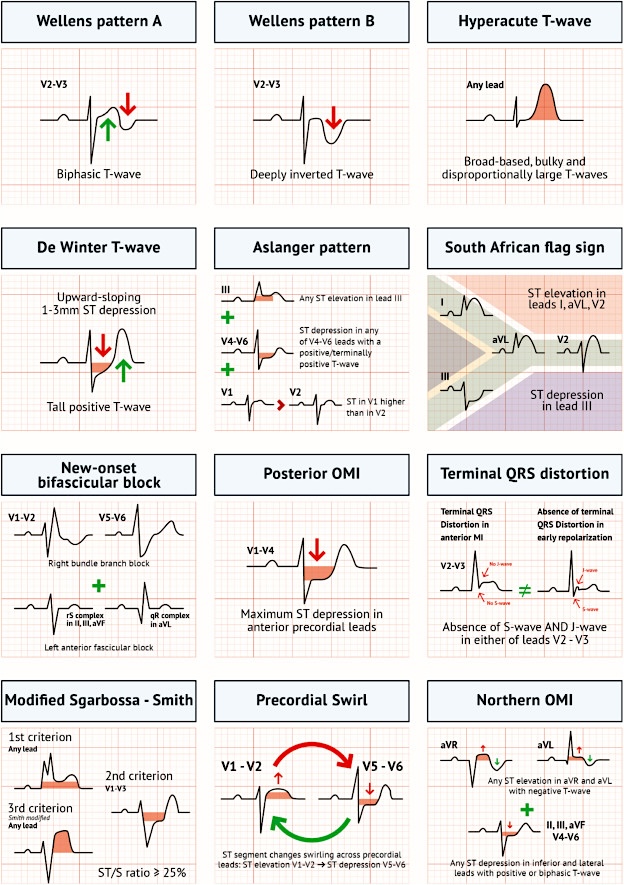
ECG normal ?

Réponse: NON. En V2-V3, les ondes r sont chétives, rabotées et en V1-V3 les ondes T sont un peu trop amples (dépassant R). Des petites anomalies de la repolarisation sont visibles en V6-D1 et en territoire inférieur. Occlusion de l’IVA rapidement détectée par l’évolution des ECG et l’élévation de la troponine.
- La reproductibilité des interprétations d’ECG tests pour l’évaluation du SCA est souvent décevante [24][25][26][27].
La lecture de l’ECG est biaisée par la clinique
- La clinique est plutôt évocatrice de SCA, on a alors tendance à davantage prendre en considération des indices ECG d’ischémie coronaire compatibles avec son hypothèse clinique (« expectation biais ») et à ignorer les indices non concordants qui orientent vers d’autres hypothèses (biais de confirmation) [28].
- La clinique est plutôt non évocatrice de SCA, on a alors tendance à négliger certains indices subtils d’ischémie coronaire ou à ne pas répéter les tracés ECG en présence d’anomalies douteuses ou indatables (biais d’ancrage).
Pièges
- L’ECG est normal, puisqu’il a été enregistré « post critique », une fois que le patient était devenu asymptomatique, ou parce que l’anomalie ischémique aiguë enregistrée per critique n’est pas bien explorée par un ECG 12 dérivations, ou encore parce qu’elle annule l’anomalie du tracé de base (pseudonormalisation).
- La troponine initiale est trop précoce ou passe sous les radars de détection car les symptômes ont été brefs (Indispensable. Unstable Angina Still Exists in Era of high sensitivity troponin).
- Des troubles du rythme (ex. ESV, RIVA ou bloc de branche gauche) sont sur le « devant de la scène » et masquent les signes d’occlusion coronaire (cf. Infarctus et trouble du rythme).

Les interprétations ECG par les ordinateurs actuels ≤ 2023 sont mauvaises
 Les algorithmes ne sont pas suffisamment fiables pour la détection et la datation des petit(e)s ischémies/infarctus. Ils qualifient trop souvent de « tracé normal » ou de « non significatives » des petites anomalies évocatrices, voire caractéristiques d’une ischémie myocardique aiguë pour un clinicien bien formé. Inversement, ils jugent trop souvent des petites anomalies « compatibles avec une ischémie coronaire » alors qu’elles n’ont pas de valeur sémiologique d’orientation [29][30] ou qu’elles sont dues à d’autres causes (ex. Brugada, bloc de branche, inversion d’électrode, HVG, embolie pulmonaire…) [31].
Les algorithmes ne sont pas suffisamment fiables pour la détection et la datation des petit(e)s ischémies/infarctus. Ils qualifient trop souvent de « tracé normal » ou de « non significatives » des petites anomalies évocatrices, voire caractéristiques d’une ischémie myocardique aiguë pour un clinicien bien formé. Inversement, ils jugent trop souvent des petites anomalies « compatibles avec une ischémie coronaire » alors qu’elles n’ont pas de valeur sémiologique d’orientation [29][30] ou qu’elles sont dues à d’autres causes (ex. Brugada, bloc de branche, inversion d’électrode, HVG, embolie pulmonaire…) [31].
Les algorithmes ne sont pas non plus aptes à identifier des signes d’ischémie aiguë en cas de tracé très anormal (tachycardie, complexes QRS larges, pacemaker, hypertrophie ventriculaire, etc.).
There are two ways to write error-free programs; only the third one works. Alan J. Perlis
NB. L’intelligence artificielle a fait de très gros progrès dans la reconnaissance des occlusions coronaires avec ou sans sus-décalage de ST (cf. Queen of Hearts).
–>Vidéo YouTube (P. Taboulet, dec 2022, 59 min) : Pourquoi le diagnostic ECG d’un infarctus (SCA) est difficile ?
Vidéos sur YouTube (voir liste ici)
Technique de lecture, ECG difficile, pièges et références… réservés aux abonnés
Si vous souhaitez améliorer ce contenu, merci de me contacter
La suite est réservée aux membres et stagiaires du site.
Se connecter | Devenir membre | Devenir stagiaire