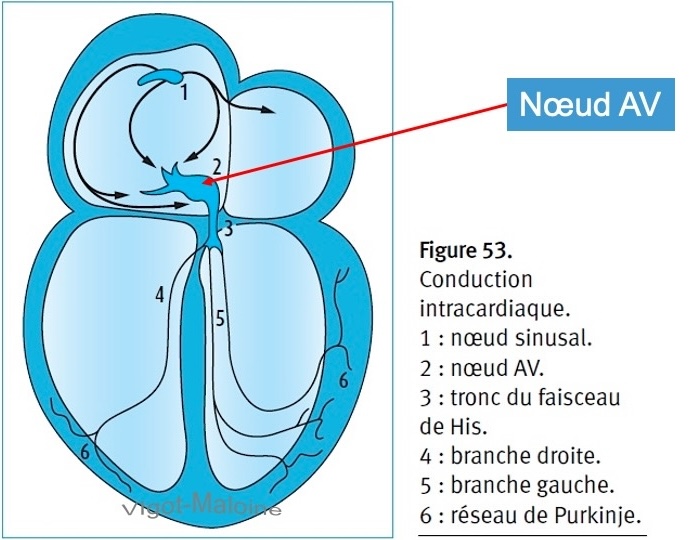
Petit nodule de fibres musculaires spécialisées, localisé près du septum interatrial, au-dessus de l’abouchement du sinus coronaire. Le nœud atrioventriculaire (NAV) est vascularisé par une artère septale inférieure venue de l’interventriculaire inférieure alimentée par l’artère coronaire droite (90%) ou circonflexe (10%).
Synonymes : nœud d’Aschoff-Tawara, nœud jonctionnel
Physiologie
Le NAV reçoit puis ralentit l’influx d’origine atriale. Celui-ci est ralenti en raison des propriétés particulières des fibres qui le constituent. Ces fibres à réponse lente ont une période réfractaire très longue qui assure un ralentissement de la conduction entre les oreillettes et les ventricules.
Cette conduction décrémentielle vers le faisceau de His permet un remplissage ventriculaire efficace sur le plan hémodynamique (la systole atriale permet un bon remplissage ventriculaire avant la systole ventriculaire). Elle confère aussi au NAV un rôle de filtre qui permet de prévenir une stimulation trop fréquente des ventricules en cas de tachycardie atriale.
ECG et ECG endocavitaire
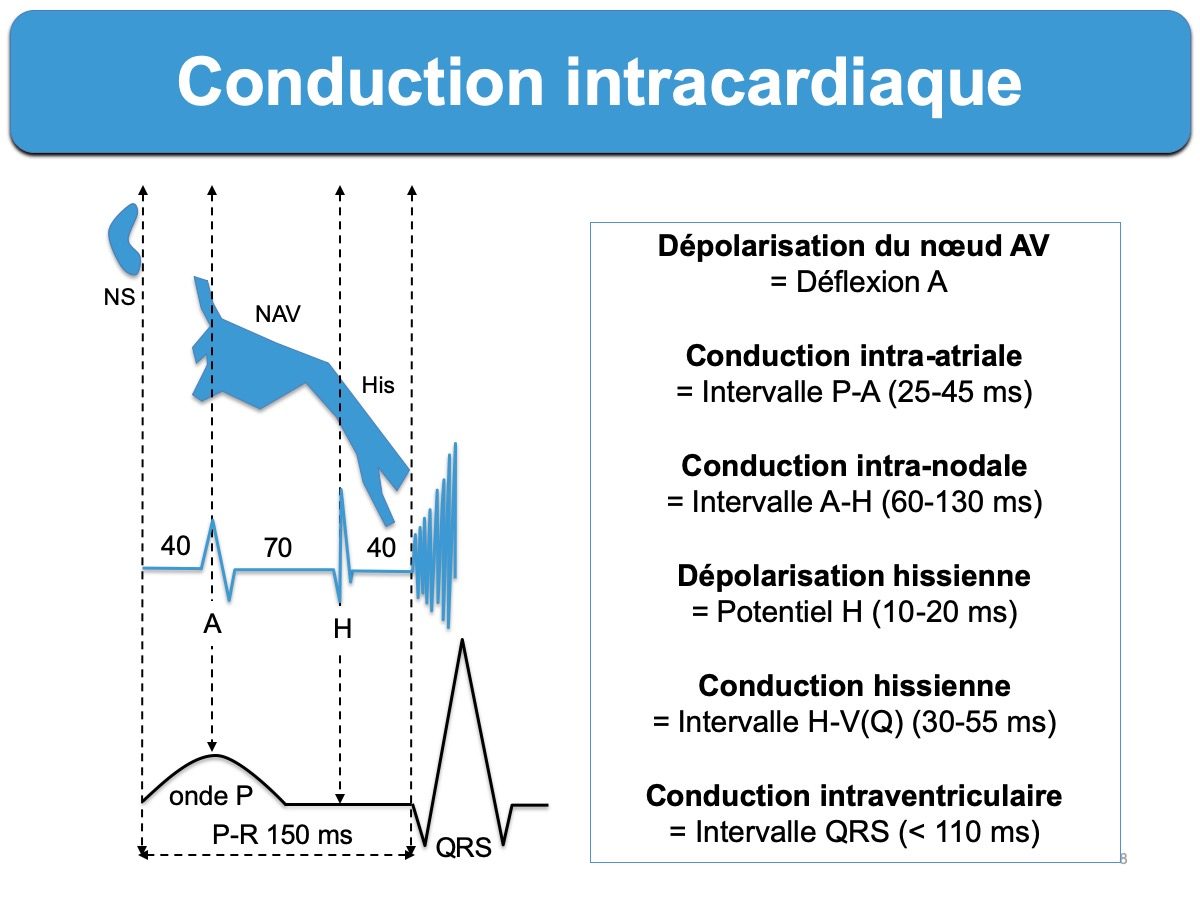
La traversée du nœud correspond sur l’ECG à la partie terminale de l’onde P et la majorité du segment PR (cf. Activation électrique du cœur). L’intervalle PR est physiologiquement compris entre 120 et 200 ms, mais il est plus court chez environ 2% de la population en cas de « nœud hyperdromique ». Cette variante est caractérisée par un intervalle P-R court (< 120 ms) qui s’allonge quand la fréquence atriale augmente. Le diagnostic différentiel est une préexcitation ou une conduction nodale accélérée (cf. syndrome du PR court).
Les propriétés électrophysiologiques du NAV s’explorent au cours d’un ECG endocavitaire.
Physiopathologie
L’influx traverse le nœud physiologiquement de façon antérograde en utilisant un circuit court. Il peut aussi utiliser un circuit long. Ces deux circuits ne correspondent pas à des voies anatomiques différentes, mais des circuits fonctionnels du fait d’une anisotropie de la région. Cette dualité nodale peut être à l’origine de tachycardie par réentrée intranodale (cf. voir microréentrée, Bouveret).
Le nœud AV reçoit parfois un influx d’origine ventriculaire et peut le bloquer ou le conduire de façon rétrograde aux oreillettes. Cette conduction rétrograde s’observe dans certains cas de rythme infranodal et en cas de conduction antidromique (cf. Tachycardie antidromique).
La fibrose des voies de conduction (cf. Cardiomyopathie atriale, Maladie de Lenègre, Maladie rythmique de l’oreillette…) ou un infarctus atrial (cf. Infarctus et bloc AV) peuvent entraîner un dysfonctionnement du NAV à l’origine d’un bloc AV du 1er, 2e degré Mobitz 1 ou 3e degré parfois sensible à l’atropine.
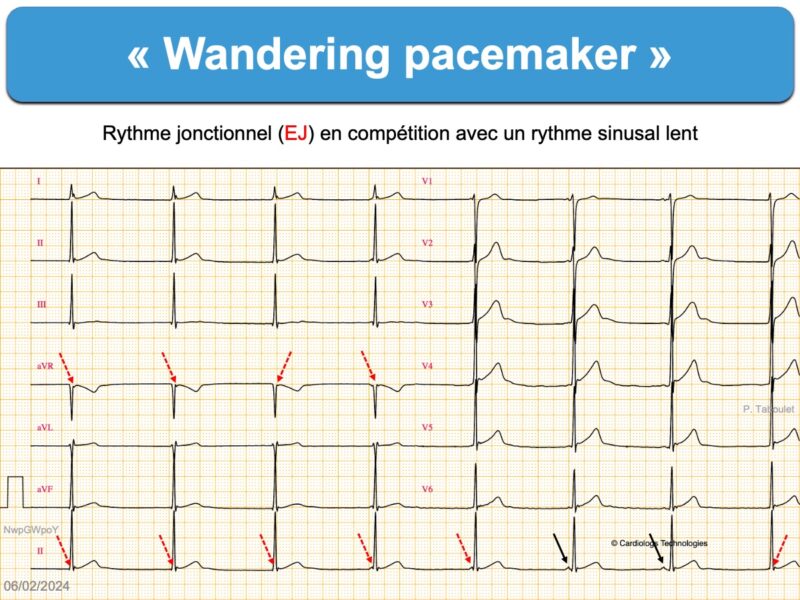
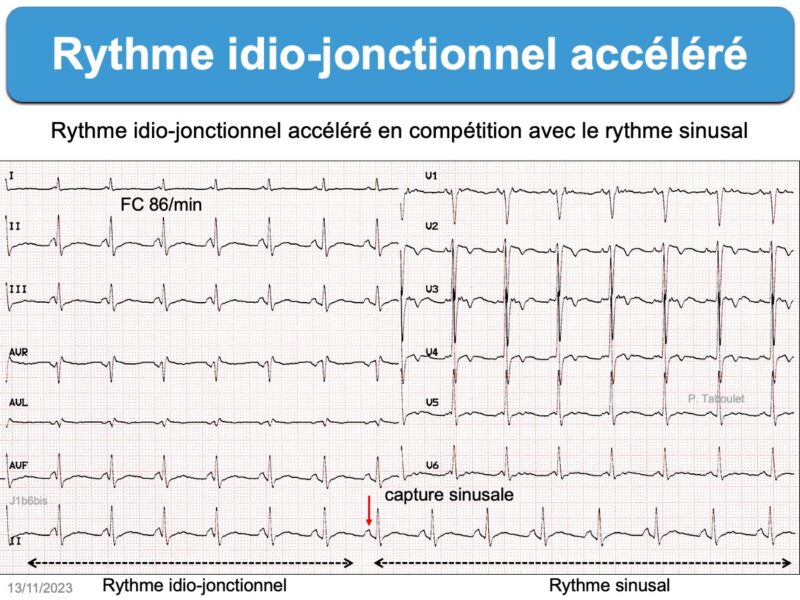
Les cellules du NAV sont douées d’automatisme et peuvent prendre la commande du rythme cardiaque en cas de bradycardie sinusale ou de bloc sinoatrial (cf. Wandering pacemaker, bloc sino-atrial, Rythme d’échappement) ou de circonstances à l’origine d’un hyperautomatisme de la jonction atrioventriculaire* (cf. Rythme idiojonctionnel accéléré ou Tachycardie atrioventriculaire automatique non réentrante).
*La jonction atrioventriculaire inclut le nœud AV et le tronc du faisceau de His